-
- 產品搜尋
- 會員登入/註冊
- 關於新國
- 代理品牌
- 產品資訊
- 全球據點
- 研究發展
- 技術支援
- 新聞中心
- 會員專區
- 網站地圖
- 聯絡我們
- 公司據點
- 繁中 EN

淺談紫外光可見光光譜原理/uv vis原理
UV VIS原理簡介
紫外-可見光吸收光譜法(ultraviolet and visible spectrum),是以紫外-可見光區域(通常190-1100 nm)電磁波連續光譜作為光源,照射樣品後,研究物質分子對光吸收的相對強度的方法。物質中的分子或基團,吸收了入射的紫外及可見光能量,電子間能級躍遷產生具有特徵性的紫外-可見光譜,可用於確定化合物的結構和特定化合物的性質。在化學、材料、生物、醫學、食品、環境等領域都有廣泛的應用。
圖1. Thermo Fisher Evolution系列紫外光可見光光譜儀
物質的吸收光譜,本質上就是物質中的分子吸收了入射光中某些特定波長的光能量,並相應地發生躍遷的結果。紫外-可見吸收光譜就是物質中的分子或基團,吸收了入射的紫外可見光能量,產生了具有特徵性的帶狀光譜。
分子光譜的產生以及類型
分子中有電子的移動,各原子間的振動,以及分子作為整體的轉動,這三種不同的運動狀態都對應一定的能階。光和物質相互作用時,分子中電子能階、振動能階和轉動能階產生變化,使分子對光產生了吸收、發射或散射,從而得到分子光譜。分子從外界吸收光能,從基態躍遷到激發態,把被吸收的輻射強度按波長順序記錄下來,便得到吸收光譜,如圖2所示。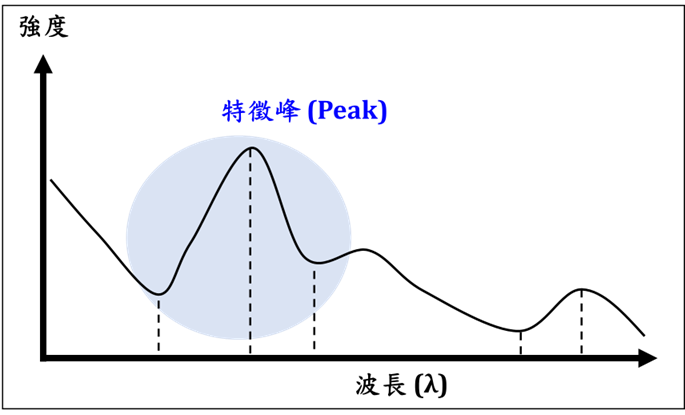
圖2. 吸收光譜示意圖
根據電磁輻射的波長範圍和作用形式的不同,見下圖3所示,分子光譜包括紫外-可見光譜、紅外光譜、微波光譜、螢光光譜和拉曼光譜等。
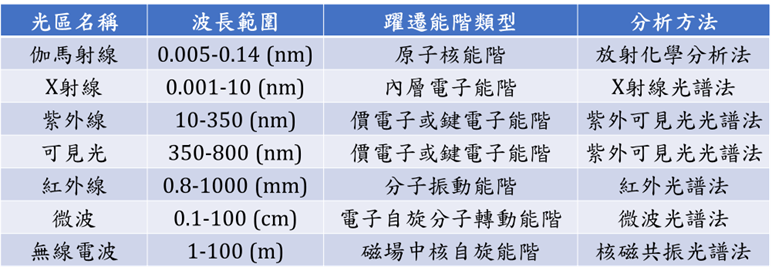
圖3. 光譜分類
紫外可見吸收光譜的電子躍遷
有機化合物的紫外吸收光譜:基態有機化合物的價電子包括成鍵δ電子、成鍵π電子和非鍵電子n。分子的空軌道包括反鍵δ*和反鍵π*軌道。因此,可能得躍遷為δ→δ*、π→π*、n→δ*、n→π*等。由圖4可見,各種躍遷所需能量大小為:δ→δ*>n→δ*≥π→π*>n→π*。 圖4. 有機化合物中電子躍遷類型
圖4. 有機化合物中電子躍遷類型
無機化合物的紫外吸收光譜:①電荷遷移躍遷:化合物中的電荷發生重新分佈,導致電荷從化合物的一部分遷移至另一部分。②配位場躍遷:在配位的配位場作用下,產生d→d*和f→f*躍遷。當過渡金屬離子與顯色劑形成鉗合物時,既存在電荷轉移吸收,又存在著配位體吸收。
比爾定律(Beer’s Law)
如圖5所示,當一平行單色光束照射溶液時,一部分光會被溶液吸收,另一部分被介面反射,其餘的光則穿透過溶液。將穿透射光強度(It)與入射光強度(I¬0)的比值It / I¬0稱為穿透率(Transmittance, %T)。溶液對光的吸收程度常用吸收度(Absorbance, A)表示。吸收度A定義為穿透率的負對數,即A = -log T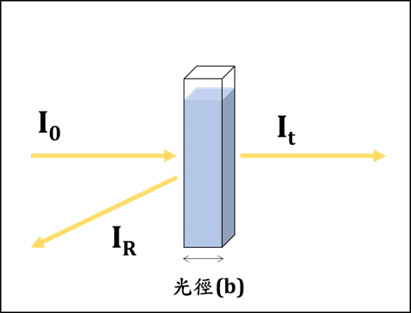
圖5. 光通過溶液的情況
比爾定律的物理意義是當一束平行單色光通過單一均勻的、非散射的吸光物質溶液時,溶液的吸收度(A)與光徑(b)和溶液濃度(c)的乘積成正比。如果物質中只有一種吸收成分,則朗伯-比耳定律的數學運算式為A=a·b·c,吸收係數a與入射光的波長以及吸收物質的性質有關,a的單位為L/g·cm。若濃度的單位為mol/L,則a的單位為L/mol·cm,也稱為摩爾吸收係數ε。
紫外光可見光光譜儀儀器結構
光譜儀是由光源、分光系統(單色器)、比色槽、偵測器和測量訊號顯示系統(記錄裝置)這五個基本部件組成的,如圖6所示。由光源產生的複合光通過單色器分散為單色光,當單色光通過比色槽時,一部分光被樣品吸收,未被吸收的光到達接收放大器,將光訊號轉變成電訊號並加以放大,放大後的電訊號再顯示或記錄下來。 圖6. 紫外光可見光光譜儀設計架構
圖6. 紫外光可見光光譜儀設計架構
(1)光源:鎢絲燈和氘燈。
(2)分光系統:將光源發射的複合光分解成單色光並可從中選出任一波長單色光的光學系統,主要由狹縫、色散原件和透鏡系統組成。
(3)比色槽:又稱比色皿,用於盛裝待測溶液和光徑厚度的器件。主要由石英製或塑膠製兩種。石英製可用於紫外及可見光區,塑膠製只能用於可見光區。
(4)偵測器:利用光電效應將透過比色槽的光訊號轉變為電訊號。常用的有光電管、光電倍增管、光電二極體、光電攝像管等。

